Diagnostic clinique
Marche à suivre pour obtenir un diagnostic complet dans les cas de MHR
It looks like you are using an older version of Internet Explorer which is not supported. We advise that you update your browser to the latest version of Microsoft Edge, or consider using other browsers such as Chrome, Firefox or Safari.
Marche à suivre pour obtenir un diagnostic complet dans les cas de MHR
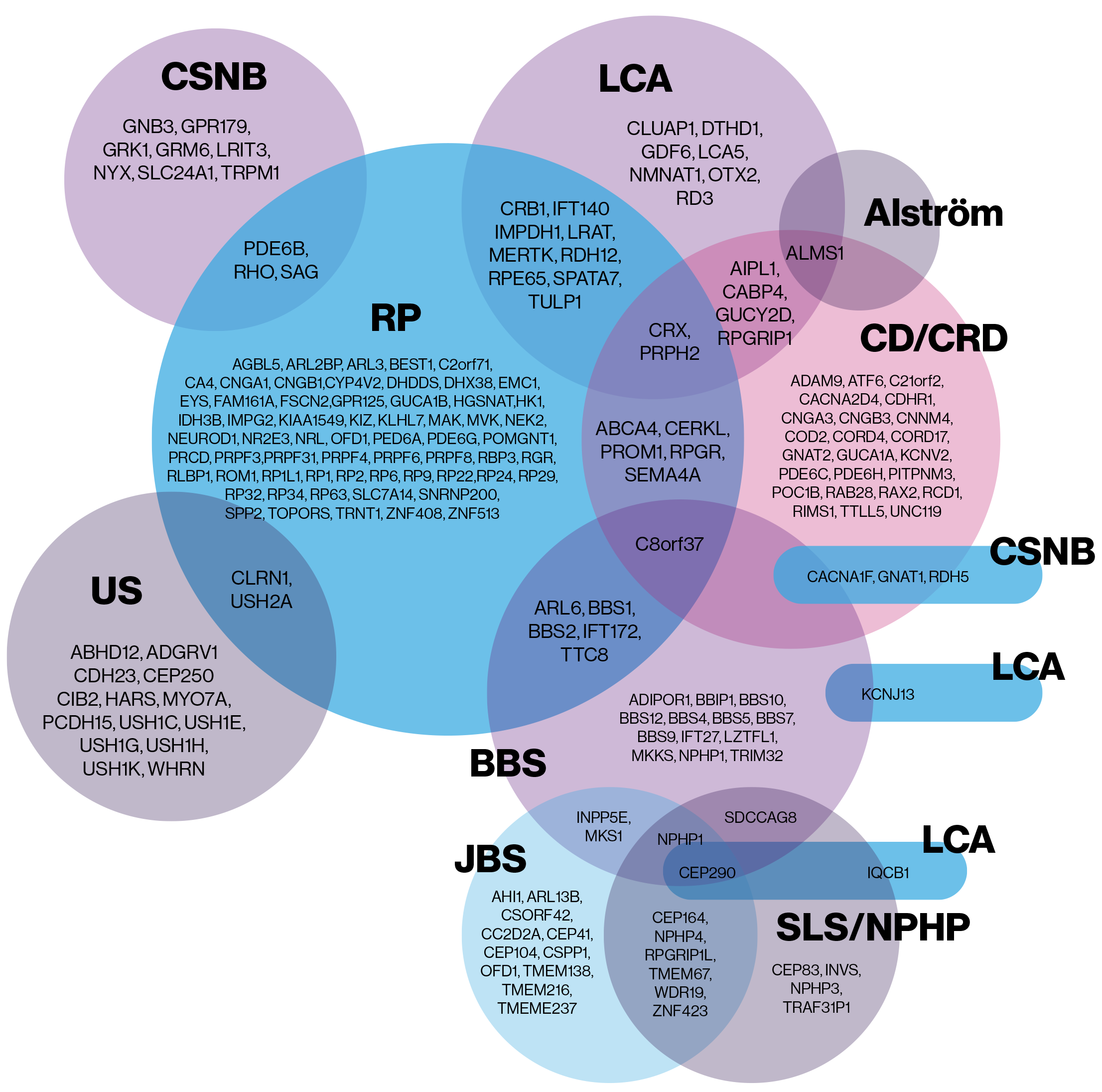
Les dystrophies rétiniennes peuvent être classées de plusieurs façons, notamment selon qu’il s’agit d’un syndrome (maladie qui touche d’autres appareils ou systèmes tels que le syndrome d’Usher) ou non (dont les symptômes sont uniquement de nature visuelle) et en fonction du principal sous-type de cellules qui sont fragilisées1-4.
Lorsque ce sont les bâtonnets qui sont touchés plus gravement, la vision nocturne ou dans la pénombre et la vision périphérique s’affaibliront avant que la vision centrale et celle des couleurs ne se détériorent. En revanche, lorsque ce sont les cônes qui sont surtout fragilisés, les principaux signes de maladie peuvent être une photophobie, une mauvaise vision centrale et une vision altérée des couleurs qui se manifestent avant que l’aggravation de la déficience visuelle ne devienne évidente3.

D’après le site Web de Vaincre la cécité Canada et l’Atlas of Inherited Retinal Diseases2,5.
Cette vidéo présente le cas d’une patiente et de sa famille qui découvrent les symptômes d’une MHR et qui prennent connaissance du diagnostic. Les membres de la famille expliquent les raisons qui les ont poussés à subir un dépistage génétique et ce qu’ils ont vécu après en avoir reçu les résultats.
Comme les maladies regroupées sous l’appellation maladies héréditaires de la rétine sont nombreuses, l’éventail de leurs signes et symptômes est large et comprend une baisse de la vision nocturne, de la vision des couleurs et de l’acuité visuelle centrale et une amputation du champ visuel3,6. Parmi les premiers symptômes évoquant une MHR, on trouve les suivants :

Chez les bébés et les jeunes enfants

Chez les enfants plus vieux, les adolescents et les adultes
Cette vidéo jette un éclairage sur ce qu’est la vie avec une MHR, sur les soins à donner à une personne qui en est affligée et sur certains symptômes.
Méthode d’examen faisant appel à des électrodes cutanées pour les jeunes enfants et à des électrodes intégrées à des lentilles de contact pour les enfants plus vieux et les adultes. Des stimuli lumineux sous forme de flashs et de clignotements d’intensité et de fréquence variables sont envoyés dans les yeux pour évaluer la réaction et le fonctionnement des photorécepteurs2,8,9.

La lipofuscine est un fluorophore qui s’accumule dans l’épithélium pigmentaire de la rétine et qui peut servir de marqueur de substitution de l’activité photoréceptrice en étant mis en évidence par autofluorescence du fond d’œil. Selon le schéma de fluorescence obtenu, il est alors possible d’orienter le diagnostic vers une maladie en particulier2.

La TCO fait appel à la réflexion de la lumière pour visualiser la structure des différentes couches de la rétine dans ses moindres détails. Elle peut être utilisée pour mesurer l’épaississement de la rétine et pour évaluer l’état d’avancement des dystrophies rétiniennes2,10.

Auparavant, le diagnostic des MHR reposait essentiellement sur les examens cliniques. Or, de nouvelles méthodes de dépistage ont récemment été mises au point de sorte que l’intérêt pour certaines mutations génétiques s’est aiguisé3,8.
Le dépistage génétique? De quoi s’agit-il?
Il s’agit d’un examen médical qui permet d’étudier l’ADN humain et qui sert à déceler des modifications, ou mutations, génétiques susceptibles de donner lieu à des maladies héréditaires. Le dépistage génétique est réalisé à partir d’échantillons d’ADN habituellement extrait du sang ou de la salive et consiste à séquencer l’ADN afin d’en répertorier les mutations. La plupart du temps, on se concentre sur une batterie de quelques centaines de gènes que l’on sait être mutés dans les cas de MHR2,11.
Décision à prendre : votre patient devrait-il subir un dépistage génétique?
Il convient de faire subir un dépistage génétique à la plupart des patients atteints d’une dégénérescence rétinienne présumée être d’origine héréditaire8.
Il faut l’envisager si :
Le patient présente les signes et les symptômes d’une MHR

Autres appareils ou systèmes :
Une dystrophie rétinienne héréditaire a été diagnostiquée chez le patient ou ce dernier a des antécédents familiaux de MHR8,11
Si vous soupçonnez que votre patient est atteint d’une MHR, envisagez de lui faire subir un dépistage génétique le plus tôt possible. Le temps d’attente pour cet examen peut être de 1 à 2 ans.
Le dépistage génétique vous fournira un complément d’information sur la MHR de votre patient. C’est le seul moyen de savoir quels gènes sont mutés, ce qui peut aider à poser un diagnostic2,8,11. Les patients qui reçoivent un diagnostic de maladie héréditaire pourraient tirer avantage d’une consultation avec un conseiller en génétique. La marche à suivre pour demander un dépistage génétique peut varier d’une province à une autre et peut se révéler complexe, mais elle comprend généralement les étapes suivantes3,5 :
1. Après avoir posé un diagnostic provisoire, un ophtalmologiste ou un autre médecin spécialisé en médecine génétique prend des dispositions pour procéder au dépistage. En cliquant sur l’hyperlien ci-dessous, vous obtiendrez la liste des cliniques de dépistage génétique en fonction de votre adresse, ainsi que les formulaires de consultation correspondants :
Cliniques de dépistage génétique provinciales :
https://www.cagc-accg.ca/index.php?page=225&id=&locale=fr_CA
2. Un conseiller en génétique rencontre le patient pour lui expliquer la raison d’être, les avantages, les risques et les inconvénients du dépistage génétique, ainsi que les résultats qui en ressortent.
3. L’échantillon d’ADN analysé provient du sang ou de la salive du patient; le dépistage et les consultations peuvent prendre plusieurs mois, voire des années, suivant la province de résidence.
4. Si les résultats de l’analyse d’une première batterie de gènes ne sont pas concluants, on peut séquencer l’exome en entier afin d’augmenter la probabilité de diagnostiquer une maladie génétique, car plusieurs gènes sont mis en cause dans les MHR.
ERG = électrorétinogramme